DSC 피크 해석: 상변화와 화학반응 분석
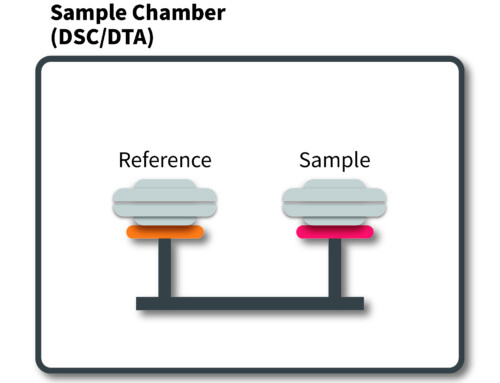
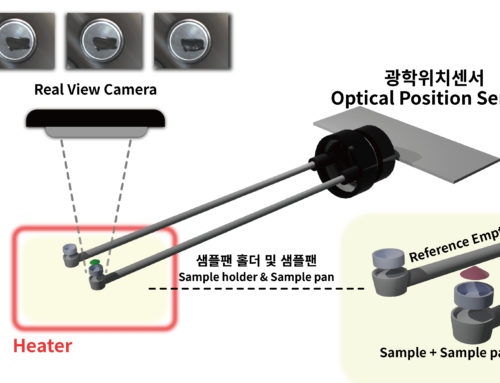
DSC를 통한 소재의 상변화 또는 화학 반응의 확인
DSC를 통한 소재의 상태 변화 및 기타 화학 반응의 확인
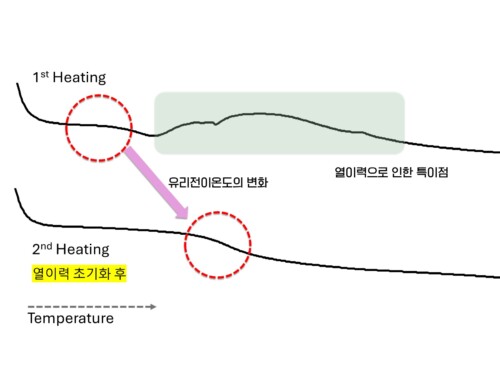
지난 포스팅에서는 DSC를 통한 고분자 소재의 유리전이온도(Glass transition temperature)를 확인하는 방법에 대해 소개했습니다. (참고링크: DSC 결과 해석 유리전이온도)
유리전이온도와 더불어 DSC분석을 통해 확인할 수 있는 것이 상태 변화와 화학반응입니다. 대표적으로 녹는점과 에폭시 등의 열경화 등을 예로 들 수 있습니다. 상변화와 반응의 큰 특징은 변화 중 에너지를 흡수하거나 방출한다는 것입니다. 이것을 흡열(Endothermic) 또는 발열 반응(Exothermic reaction)이라고 합니다.
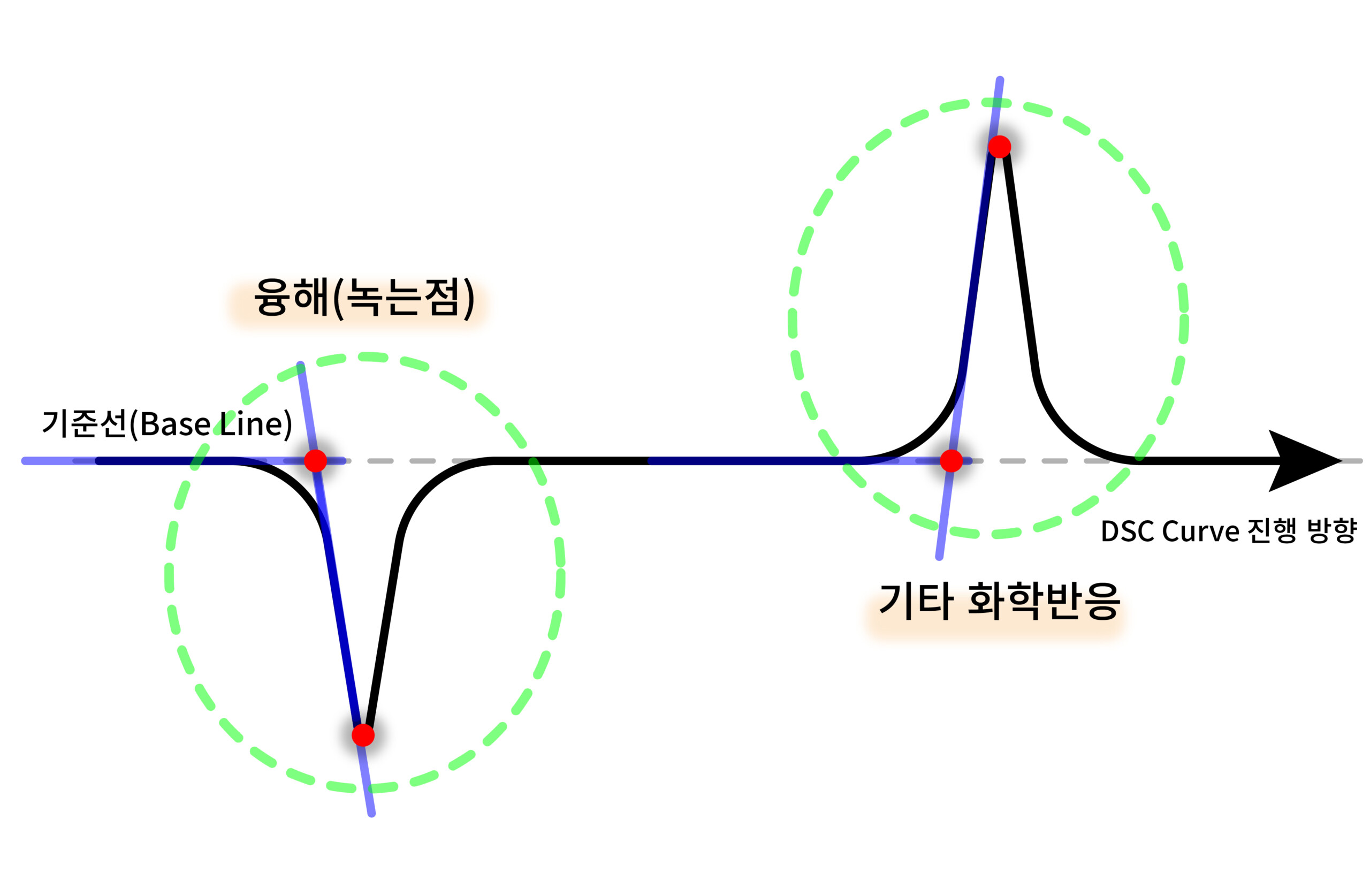
DSC 결과에서는 아래 그림과 같이 반응 전후의 기준선(Base Line)이 있고 산 모양의 피크가 생긴다는 점인데요. 이런 그래프의 개형에서 반응의 시작 점과 반응에 필요한 에너지인 엔탈피(enthalpy)를 계산할 수 있게 됩니다. 모든 반응에서 동일한 형태로 나타나는 것은 아니지만 물이나 금속과 같이 순수한 물질의 반응에서는 전형적으로 확인할 수 있는 기본 형태라고 생각하면 되겠습니다.
DSC Curve의 피크(Peak) 형태
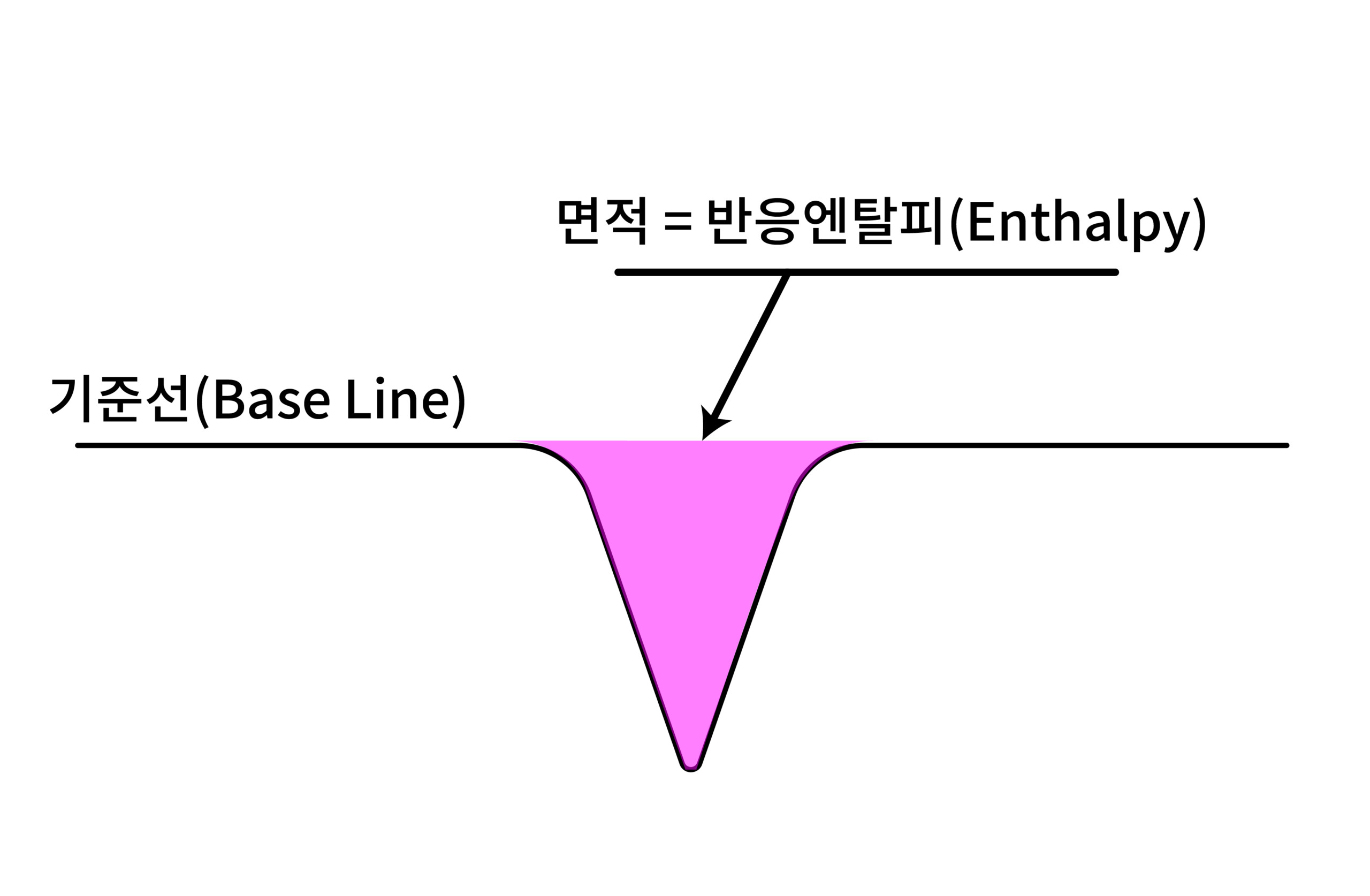
반응 DSC 피크의 해석 방법
피크를 나타내는 대표적인 반응의 형태는 융해(Melting)와 결정화(Crystallization) 그리고 기타 화학 반응이 있습니다. 해석하는 방법은 대부분 유사하며 소재의 특성에 대한 개략적인 정보를 토대로 관측된 피크가 어떤 반응인지 추정하는 것이 일반적입니다.
가열/냉각 시 DSC 결과 예시
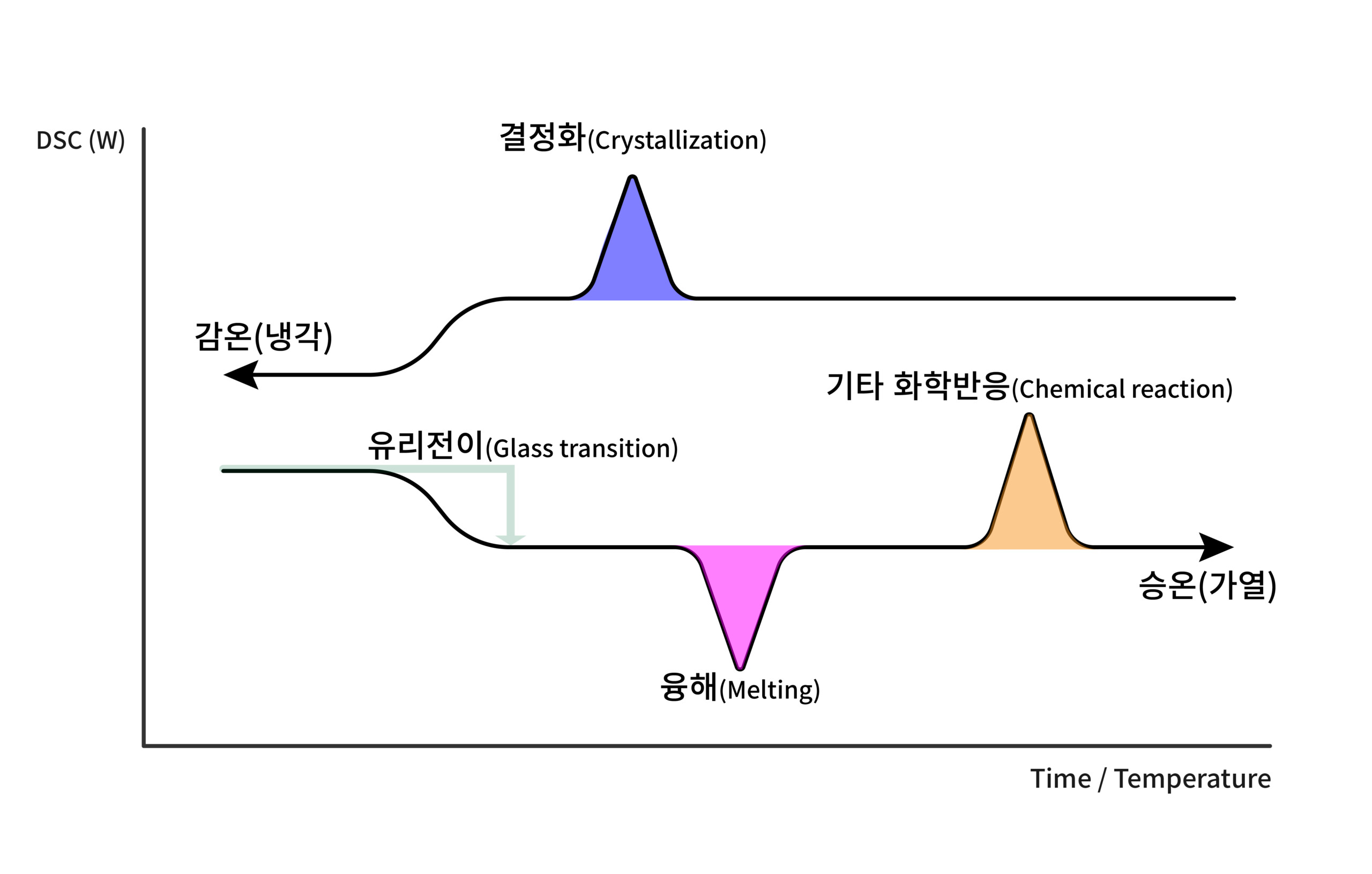
DSC 해석: 상변화
위와 같이 다양한 피크가 관찰되며 각 피크의 종류와 해석 방법은 다음과 같습니다.
| 종류 | 내용 및 특징 | 해석 |
|---|---|---|
| 융해(Melting) |
|
|
| 결정화 (Crystallization) |
|
|
| 기타 화학반응(Chemical reaction) |
|
|
그러나 소재의 특성과 화합물의 조성, 반응의 매커니즘과 종류에 따라서 매우 다양한 DSC Curve가 관찰 될 수 있습니다.
경우에 따라서는 분석의 기준이 될 수 있는 기준 물질(Reference material)을 측정하여 결과와 비교하거나 소재의 특성에 대한 정보를 사전에 알아야 분석이 가능한 경우도 있으니 유의해야 합니다.
MCC의 분석 서비스가 궁금하다면?
더 유익한 분석 정보가 필요하다면?